II. UNE « VRAIE » MALADIE QUI PEINE À ÊTRE RECONNUE
A. UNE « VRAIE »MALADIE...
L'obésité entraîne une inflammation à bas bruit délétère et altère la flore intestinale. Elle est le résultat de deux types de dérèglement :
- une défaillance des systèmes de régulation qui conduit le mangeur à surconsommer par rapport à ses besoins énergétiques ;
- une disposition du tissu adipeux qui favorise un développement plus ou moins irréversible des adipocytes.
Elle constitue une maladie car elle peut mettre en cause le bien-être somatique, psychologique et social des individus.
1. Une maladie chronique
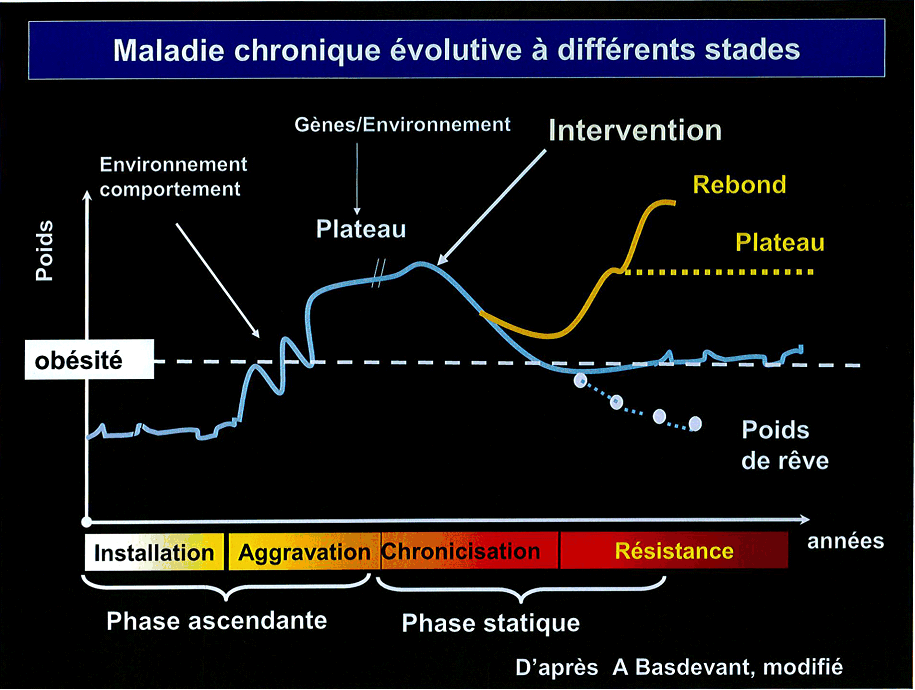
Source : Olivier Ziegler
L'obésité est une maladie chronique évolutive et les mécanismes physiopathologiques en cause varient selon le stade de l'obésité.
Dans la phase dynamique, l'augmentation initiale de la masse grasse résulte d'un déséquilibre du bilan énergétique au profit du stockage de la masse grasse. Néanmoins, durant cette phase, les dépenses énergétiques des obèses tendent à augmenter par l'accroissement de la masse musculaire concomitant à celui de la masse grasse et par une oxydation des lipides.
S'ensuit une phase statique au cours de laquelle le poids se stabilise (mais à un niveau supérieur que le niveau initial), traduisant un nouvel équilibre au niveau du bilan d'énergie.
Or, il semblerait que cette phase soit associée à une chronicisation de l'obésité qui s'avère alors difficilement réversible. En effet, le tissu adipeux se modifie, un phénomène de résistance à l'amaigrissement s'instaure et les complexités liées à l'obésité apparaissent.
a) L'altération du tissu adipeux
(1) Hypertrophie et hyperplasie
Les acides gras sont stockés dans le tissu adipeux par les adipocytes sous forme de triglycérides. Le tissu adipeux est d'une grande plasticité et reste capable de se développer tout au long de la vie. L'augmentation de la masse grasse résulte d'une augmentation de la taille des adipocytes (hypertrophie) de façon privilégiée puis probablement de leur nombre (hyperplasie) 9 ( * ) .
L'hypertrophie résulte d'une accumulation de triglycérides par les adipocytes lorsque la balance énergétique est déréglée au profit des entrées d'énergie. Lorsque la balance énergétique devient négative, les adipocytes vont se vider en libérant les triglycérides afin de fournir de l'énergie.
Par ailleurs, le nombre des adipocytes peut s'accroître dans de larges proportions. Cette hyperplasie résulte du processus d'adipogenèse qui implique un processus de prolifération des cellules progénitrices présentes dans le tissu adipeux et leur différentiation en adipocytes.
Selon l'hypothèse de la « taille critique », il existerait une taille cellulaire maximale. Ainsi, la cellule adipeuse différenciée se charge de triglycérides jusqu'à atteindre une taille critique au-delà de laquelle elle « recrute » un nouveau préadipocyte.
Le nombre de cellules adipeuses peut continuer d'augmenter si le stockage d'énergie est rendu nécessaire par un bilan énergétique positif. En revanche, une fois différenciées, les cellules ne retournent pas au stade de précurseurs. Elles restent disponibles pour stocker de nouveau des triglycérides.
Au niveau du tissu adipeux sous-cutané, il semble que la première phase est celle d'hypertrophie suivie par la phase d'hyperplasie. Il faut préciser qu'au niveau du tissu adipeux viscéral, les adipocytes sont plus petits et les phases d'hypertrophie et d'hyperplasie sont encore mal définies.
(2) L'altération de la capacité d'expansion du tissu adipeux
L'hypertrophie adipocytaire génère des changements d'activités de l'adipocyte qui va produire plus de leptine par exemple mais également plus de facteurs inflammatoires. L'adipocyte hypertrophique est également moins "actif" d'un point de vue métabolique.
Cependant si cette "baisse" d'activité métabolique est compensée par la mise en place du phénomène d'hyperplasie adipocytaire qui va conduire à l'apparition de petits adipocytes "jeunes et très actifs", le tissu va continuer à assurer ses capacités de stockage.
En revanche, si la phase d'hyperplasie ne peut pas prendre le relais de la phase d'hypertrophie, le tissu adipeux va voir ses capacités de stockage du surplus d'acides gras diminuées et les acides gras vont se déposer dans d'autres tissus (foie, muscles, pancréas, coeur etc) au sein desquels ils vont avoir des effets délétères.
A l'heure actuelle, la science n'est pas en mesure de prédire la capacité d'expansion du tissu adipeux chez les patients. Si cette information devenait disponible, elle permettrait de détecter les patients qui présentent une capacité d'expansion du tissu adipeux réduite et qui, par conséquent, risquent de développer des pathologies associées à l'obésité.
La question de l'hypertrophie et de l'hyperplasie des adipocytes reste un sujet de recherche avec de nombreuses inconnues. Ainsi, P. Arner a avancé dans une étude publiée dans Nature que les capacités de prolifération (hyperplasie) étaient surtout observée à la naissance et ce jusqu'à 20 ans environ, puis que les phénomènes d'hypertrophie dominaient.
(3) L'inflammation du tissu adipeux
Le tissu adipeux blanc est composé de plusieurs types cellulaires. Outre les adipocytes et les préadipocytes, il comporte également des macrophages, des lymphocytes et d'autres types cellulaires regroupés sous le terme de « fraction stroma-vasculaire ».
Comme le rappellent Christine Poitou et Karine Clément dans un article publié en 2007, des travaux réalisés par des équipes américaines et françaises ont montré que les tissu adipeux blanc de sujets obèses est la cible d'une accumulation macrophagique et que cette infiltration est associée à l'index de masse corporelle et à l'hypertrophie adipocytaire.
Ni les mécanismes facilitant l'infiltration macrophagique et l'activation des macrophages dans le tissu adipeux, ni les conséquences locales et systémiques de cette infiltration ne sont entièrement connus.
Néanmoins, plusieurs observations ont été réalisées, notamment par l'équipe de Karine Clément.
Au niveau tissulaire, le phénomène le plus important est l'apparition d'une fibrose induite par l'inflammation chronique. Le fort degré de fibrose du tissu adipeux d'obèse pourrait altérer la capacité de communication et la vitalité des adipocytes enchâssés dans la matrice fibrose et, par conséquent, la plasticité du tissu adipeux.
En outre, il semblerait que les macrophages exercent un puissant effet inhibiteur sur la différentiation adipocytaire. En effet, le comportement des préadipocyte placés dans un milieu contenant des macrophages activés sécrétant des facteurs proinflammatoires apparaît modifié. Ils échouent à se différencier normalement, tendent à s'allonger et à acquérir une capacité de migration. Leur signature moléculaire est de type inflammatoire et l'expression des gènes de la fibrose est également augmentée. Ces préadipocytes dysfonctionnels fabriquent des composants de la matrice extracellulaire tels que la fibronectine et le collagène.
Ces travaux d'exploration à partir de modèles cellulaires humains suggèrent donc que l'inflammation bas bruit affectant le tissu adipeux perturbe profondément la biologie des adipocytes et des préadipocytes et, par voie de conséquence, réduirait la capacité d'expansion du tissu adipeux. Une hypothèse avancée est que le tissu adipeux, dans ce cas, ne peut plus jouer son rôle protecteur de stockage des acides gras qui vont se déverser dans le sang et se concentrer dans les organes.
L'obésité devient alors une pathologie d'organes avec l'apparition des complications cardiovasculaires et de l'insulinorésistance, facteur de risque du diabète de type 2.
* 9 Cette question nourrit le débat scientifique.







